Stabilita jádra je dána počtem protonů a neutronů v něm obsažených. Zvláště stabilní jsou jádra, jejichž počet protonů a neutronů je dán tzv. magickými čísly. To jsou čísla, podle nichž se zaplňují jednotlivé energetické stavy nuklidu a při nichž jádra vykazují extrémní vlastnosti související právě se stabilitou jádra.Atomy různých prvků se liší svým atomovým číslem, které vyjadřuje počet protonů v jádře (např. atom se šesti protony je atomem uhlíku; počet elektronů v obalu je u běžného elektricky neutrálního atomu shodný s počtem protonů v jádře). Atomy jednoho prvku se mohou lišit počtem neutronů v jádře (tzv.2: Proč mají různé nuklidy téhož prvku stejné chemické vlastnosti V kterých vlastnostech se mohou lišit Stejný počet protonů v jádře ⇒ stejný počet elektronů v obalu ⇒ stejné valenční orbitaly ⇒ stejné chemické vlastnosti.
Co má atomové jádro : Atomové jádro se skládá z nukleonů (určených hmotnostním číslem A): protonů (atomové číslo Z) a neutronů (neutronové číslo N). Platí A = Z + N. Číslo Z také udává počet elektronů (atom je elektricky neutrální).
Co rozhoduje o stabilite jader
Stále se jedná o chemický prvek. Izotopy prvku se odlišují svými fyzikálními vlastnostmi, nikoliv chemickými. Rozdílný počet nukleonů v jádře způsobuje rozdílnou hmotnost a poměr mezi protonovým a neutronovým číslem, který rozhoduje o stabilitě jádra.
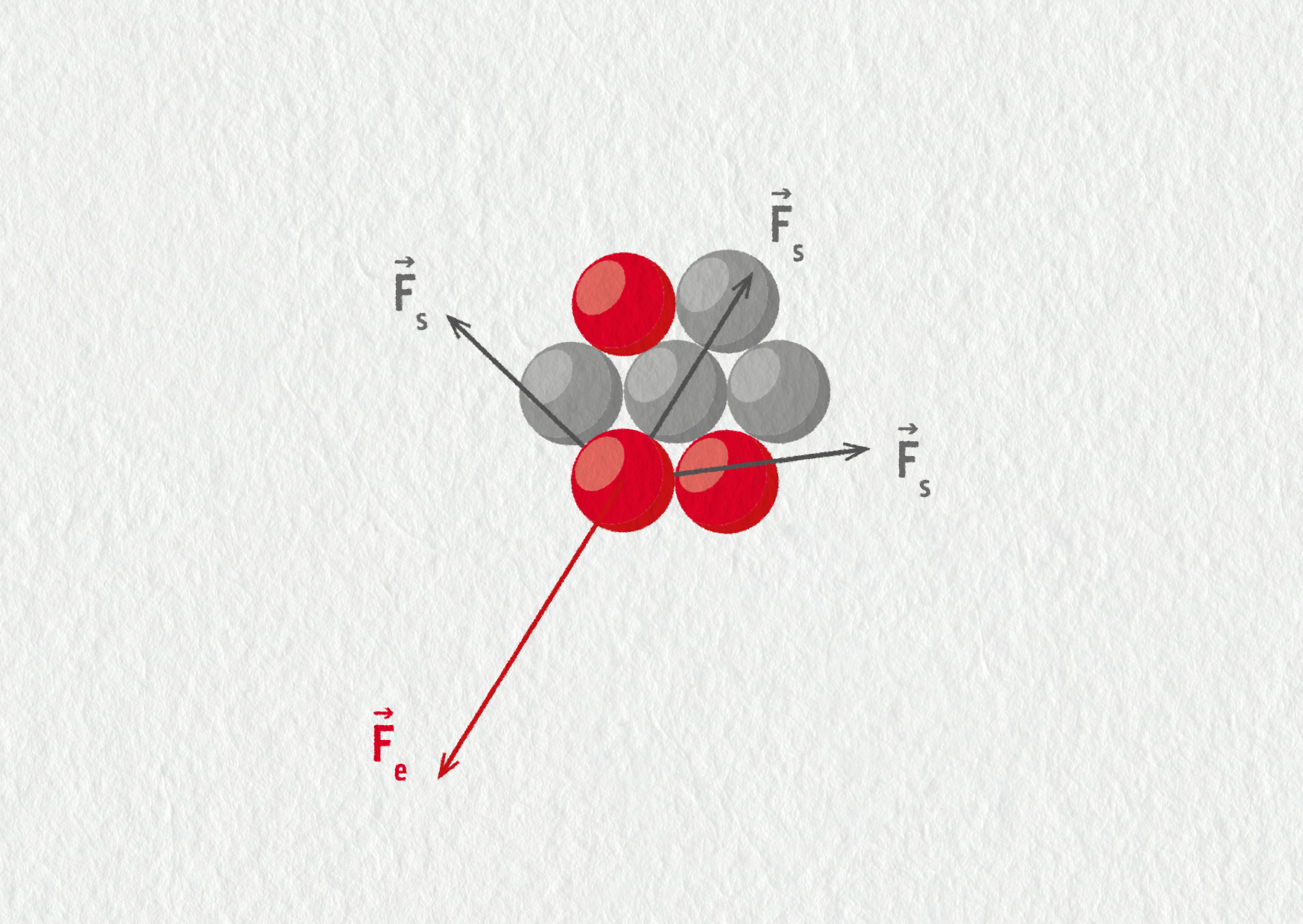
Jak pusobi jaderné sily : jsou síly působící mezi nukleony v jádře atomu. Jsou silami krátkého dosahu, který zhruba odpovídá lineárnímu rozměru jádra (řádově 10-15 m). Působí vždy jen mezi nejbližšími nukleony. Daný nukleon se tedy váže jen s omezeným počtem nukleonů, což označujeme jako nasycení jaderných sil.
Hadron je složená silně interagující subatomární částice (menší než atom). Hadrony mohou obsahovat kvarky, antikvarky, případně také gluony nebo být složeny pouze z gluonů.
“ Tento radostný výkřik zazněl v ulicích starobylého univerzitního města Cambridge v roce 1932 z úst Sira Johna Douglase Cockcrofta, když spolu s fyzikem Ernestem Thomasem Sintnem Waltonem na fluorescenčním stínítku mikroskopu zjistili přeměnu jádra lithia na dvě jádra helia.
Jaký je rozdíl mezi prvkem a Nuklidem
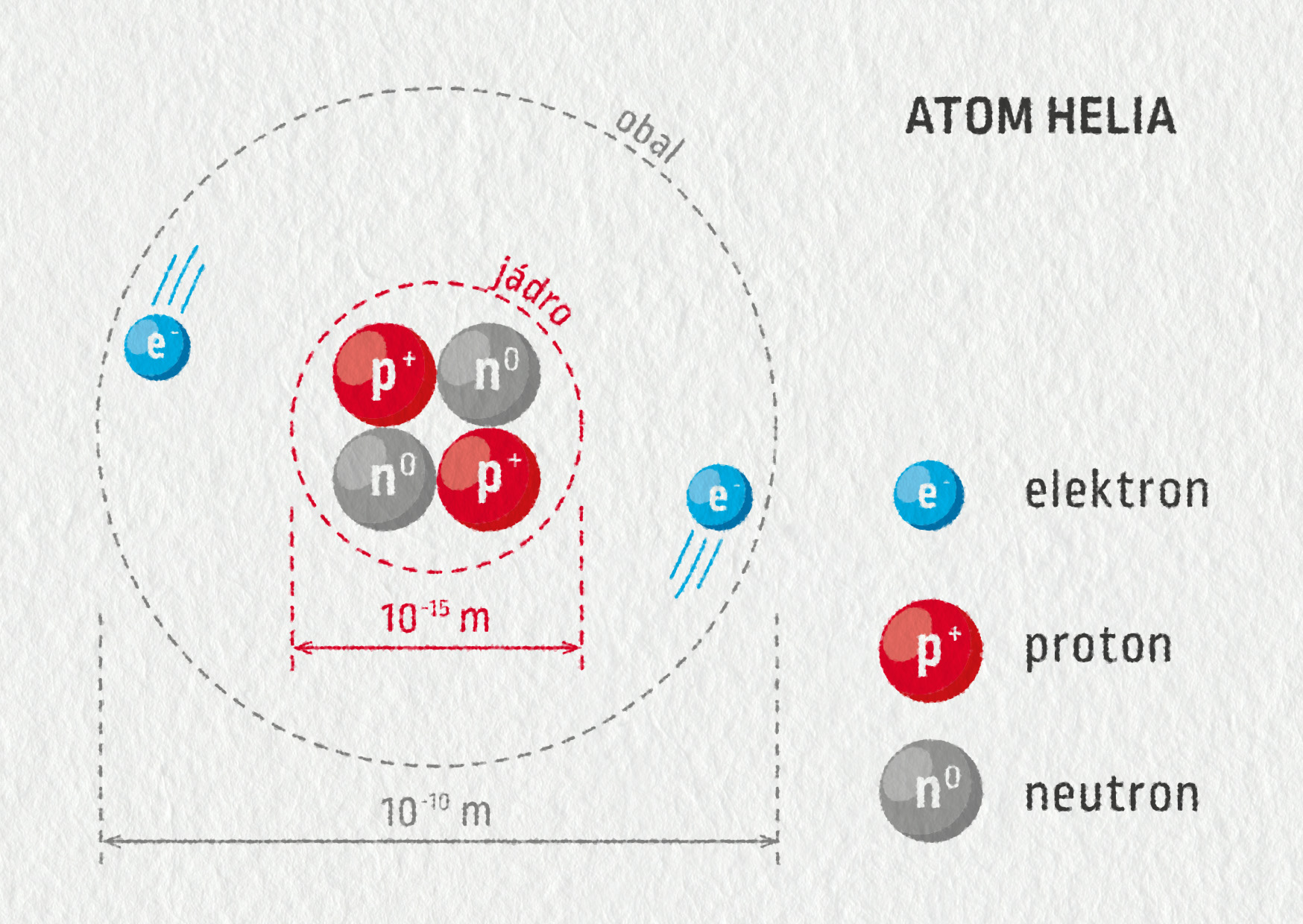
Prvek je chemicky čistá látka složená z atomů, které mají stejné protonové číslo. V čísle nukleonovém se atomy mohou i nemusí shodovat. Prvky mohou být jednoatomové, ale mohou tvořit i víceatomové molekuly. Nuklid je soubor atomů téhož prvku, které mají navzájem stejný počet neutronů (Obr.Při jaderných reakcích dochází k interakcím atomových jader s jinými jádry nebo částicemi za vzniku nových jader a emitovaných částic. Průběh konkrétních druhů jaderných reakcí bude rozebírán níže. Na několika místech budou diskutovány i analogie a rozdílnosti mezi chemickými a jadernými reakcemi.Téměř celá hmota atomu je soustředěna ve velmi malé oblasti s kladným nábojem (jádro), oblast kolem jádra má záporný náboj a zanedbatelnou hmotnost (elektronový obal). Většina objemu atomu je "prázdná", podobně jako je prázdná většina meziplanetárního prostoru.
Uvnitř jaderné zbraně implozního typu je zdroj neutronů, tzv. jaderná roznětka, to je inicializační neutronový zářič, který je sám o sobě poměrně těžko štěpitelný v řetězové reakci, avšak uvolňuje značné množství neutronů pro další štěpení, které ve vhodném okamžiku přispěje k zahájení řetězové reakce.
Kdo dokazal existenci atomového jádra : Ernest Rutherford, 1. baron Rutherford z Nelsonu, FRS (30.
srpna 1871 Brightwater, Nový Zéland – 19. října 1937 Cambridge Spojené království) byl britský fyzik novozélandského původu. Bývá považován za zakladatele jaderné fyziky.
Co se nachází v jádře atomu : Každý atom se skládá z atomového obalu a jádra. Obal je tvořen určitým počtem záporných elektronů, které si (velmi zjednodušeně) můžeme představit jako nepatrné kuličky „obíhající“ kolem kladného jádra. Jádro je složeno ze dvou druhů částic – kladně nabitých protonů a elektricky neutrálních neutronů.
Co má atomové číslo 1
S protonovým číslem souvisejí tyto termíny: Tři izotopy vodíku s protonovým číslem 1: * Protium obsahuje jeden proton a jeden elektron * Deuterium jeden proton, jeden neutron a jeden elektron * Tritium jeden proton, dva neutrony a jeden elektron Neutronové číslo (N) – je počet neutronů v jádře atomu.
Atom se skládá z atomového jádra a elektronového obalu. Jádro je proti obalu velice malé a je v něm soustředěno téměř 99 % hmotnosti celého atomu.U zrodu atomismu stál Leukippos z Milétu (asi 500 – 440 př. n.l.), jeho myšlenky rozpracoval do ucelené podoby Demokritos z Abdér (asi 460 – 370 př. n.l.). Atomisté vycházeli z představy, že náš svět se skládá z prázdného prostoru a obrovského množství neviditelných, nedělitelných, neproniknutelných částic – atomů.
Jaký je rozdíl mezi atomem a prvkem : Každý počet protonů v jádře atomu má své označení – je prvkem. Například atom, který má pouze 1 proton v jádře má označení H (vodík), prvek Zlato (Au) má v jádře 79 protonů atd. Kompletní přehled atomů nabízí PERIODICKÁ TABULKA PRVKŮ. Tak jako si například označujeme kostičky z lega.