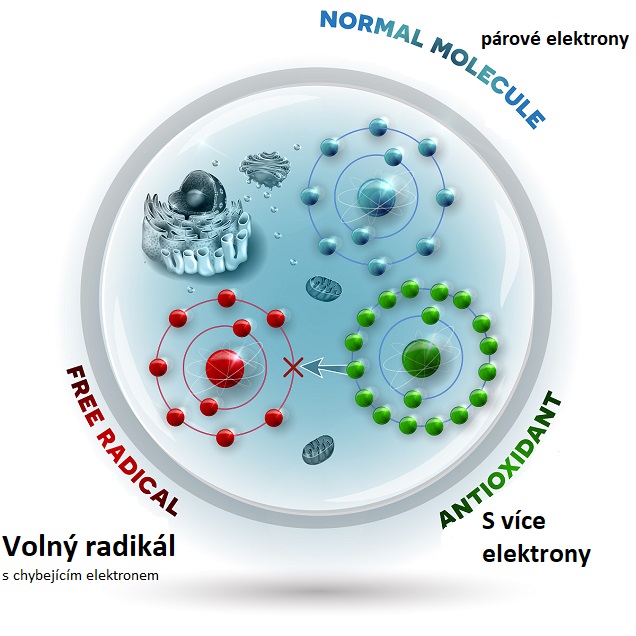
Radikál je v chemii vysoce reaktivní částice, která má jeden nebo více nepárových elektronů. Vícenásobné radikály se označují předponami; např. radikál se dvěma volnými elektrony se označuje jako biradikál.Volné radikály jsou reaktivní částice vznikající jako vedlejší produkt látkové výměny přímo v našem organismu – ať už kvůli znečištěnému ovzduší, stresu či špatné stravě. Jsou to právě volné radikály, které stojí na počátku mnoha vážných onemocnění včetně nádorových, kardiovaskulárních, plicních a imunitních.Když je ale volných radikálů velmi mnoho, tak se s nimi naše tělo nedokáže vyrovnat. Můžete si však pomoci tím, že organismu poskytneme antioxidanty. Patří mezi ně například vitamíny A, C, E, koenzym Q10, karotenoidy (beta-karoten, lutein, lykopen).
Co je Nepárový elektron : Hydroperoxylový radikál, často označovaný jen jako hydroperoxyl, je vysoce reaktivní radikál složený z dvou atomů kyslíku a jednoho atomu vodíku se souhrnným chemickým vzorcem HO2. V chemii se obvykle označuje jako HO2• – znak bullet zde jako u jiných radikálů označuje nepárový elektron.
Co to je radikál
Co jsou volné radikály a jak vznikají
Volné radikály jsou v podstatě atomy či skupiny atomů s nepárovým počtem elektronů, tedy s jedním elektronem navíc. To je činí vysoce nestabilní a reaktivní. Takovéto atomy se rychle navazují na další, kterým berou po jednom elektronu, a tak i je přeměňují na volné radikály.
Kdo je to radikál : Radikálové jsou tedy příznivci určité formy radikalismu. Výroční zpráva Royal Canadian Mounted Police z roku 2009 označuje radikála za osobu, která si přeje dosáhnout velké politické, ekonomické nebo sociální změny ve společnosti.
Oxidační stres je stav, který může nastat, když je v těle příliš mnoho nestabilních molekul označovaných jako volné radikály – a zároveň není dostatek antioxidantů, které by jich dokázaly tělo zbavit. Oxidační stres může vést k poškození buněk a tkání.
Orbital atomový
vymezují jakousi existenční oblast elektronu v atomu. Této oblasti nejpravděpodobnějšího výskytu elektronu se říká atomový orbital. Atomové orbitaly se označují symbolem obsahujícím hlavní kvantové číslo n a písmeno, které odpovídá hodnotě vedlejšího kvantového čísla l.
Co je to valenční elektron
Valenční elektrony jsou elektrony, které atomu přebývají nad konfiguraci nejbližšího předchozího vzácného plynu. Například atom kyslíku má 6 valenčních elektronů, neboť je prvkem VI. A podskupiny a přebývá mu tedy 6 elektronů nad konfiguraci předchozího vzácného plynu (helia).Radikálová substituce
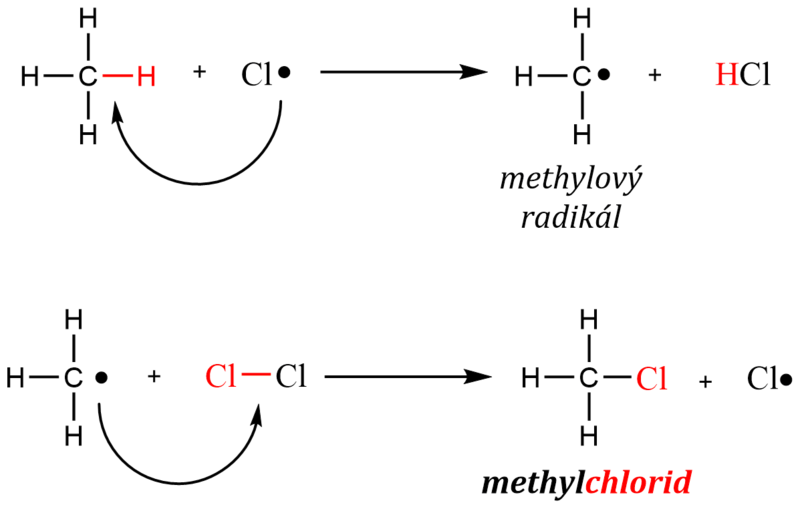
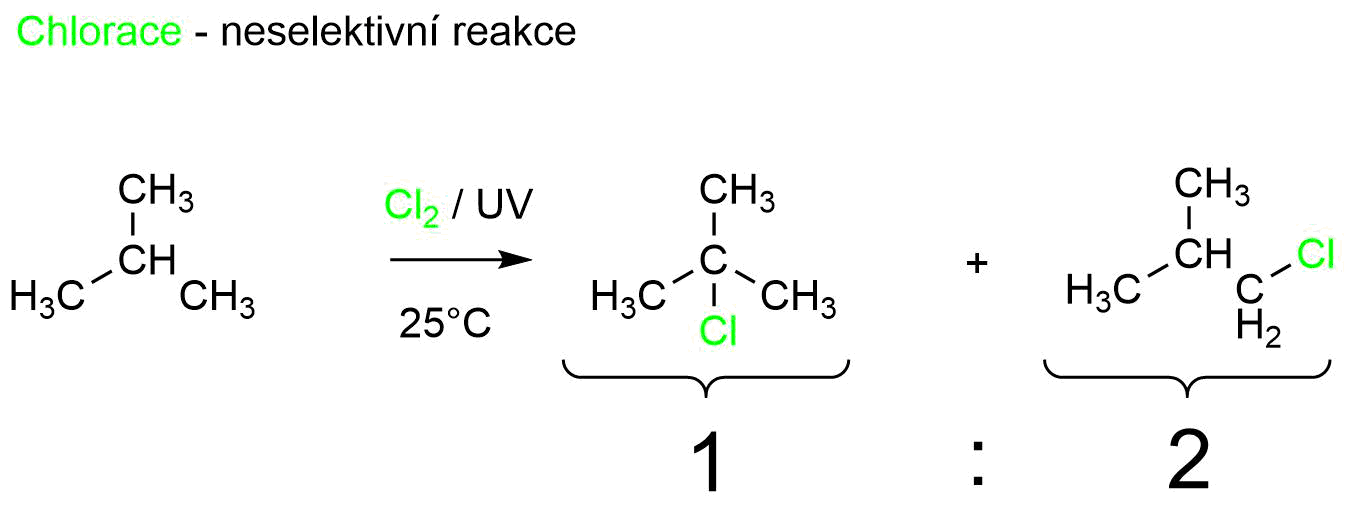
Dochází při ní k homolytickému štěpení vazeb, při kterém vznikají radikály, velmi reaktivní částice s nepárovým elektronem. Ty reagují s radikály v substituované sloučenině. Radikály jsou vysoce reaktivní, protože obsahují ve valenční vrstvě atom s lichým počtem elektronů (obvykle 7).Volné radikály jsou nestabilní molekuly, což znamená, že nemají kompletní sadu elektronů, a v důsledku toho se snaží „ukrást“ elektrony z jiných molekul. V těle kradou z buněčných membrán, a tím poškozují buňky.
Antioxidanty jsou látky, které přispívají k ochraně buněk před oxidativním stresem. Neutralizují škodlivé volné radikály a chrání tak tělo před oxidačním poškozením. Chrání buňky před působením volných radikálů tím, že se na ně naváží a neutralizují jejich aktivitu.
Co způsobuje oxidační stres : Oxidační stres může vést k poškození buněk a tkání. Existuje mnoho faktorů podílejících se na vzniku oxidačního stresu – například obezita, nevhodné složení stravy, kouření, pití alkoholu, užívání některých léků a některé vlivy životního prostředí (některé typy záření, přítomnost pesticidů, toxinů apod.).
Co způsobuje oxidaci : Oxidace povrchů začne ve chvíli, kdy se zkombinuje kyslík společně s vlhkostí. Pokud vyšší stupeň vlhkosti působí na nestabilní materiály po delší dobu, začne se snižovat jejich pevnost, snižuje se i celková trvanlivost a objevuje se koroze. U železa se setkáváme se rzí, která ovlivňuje jeho konstrukční zatížení.
Jak vypadá orbital
Orbital typu s (l = 0) má tvar koule, a tak může mít jen 1 prostorovou orientaci (m = 0). Orbital typu p (l = 1) má tvar „prostorové osmičky“, která může být v prostoru orientována podle jednotlivých souřadnicových os (x, y, z). Proto má orbital typu p přípustné 3 prostorové orientace (m = -1, 0, 1).
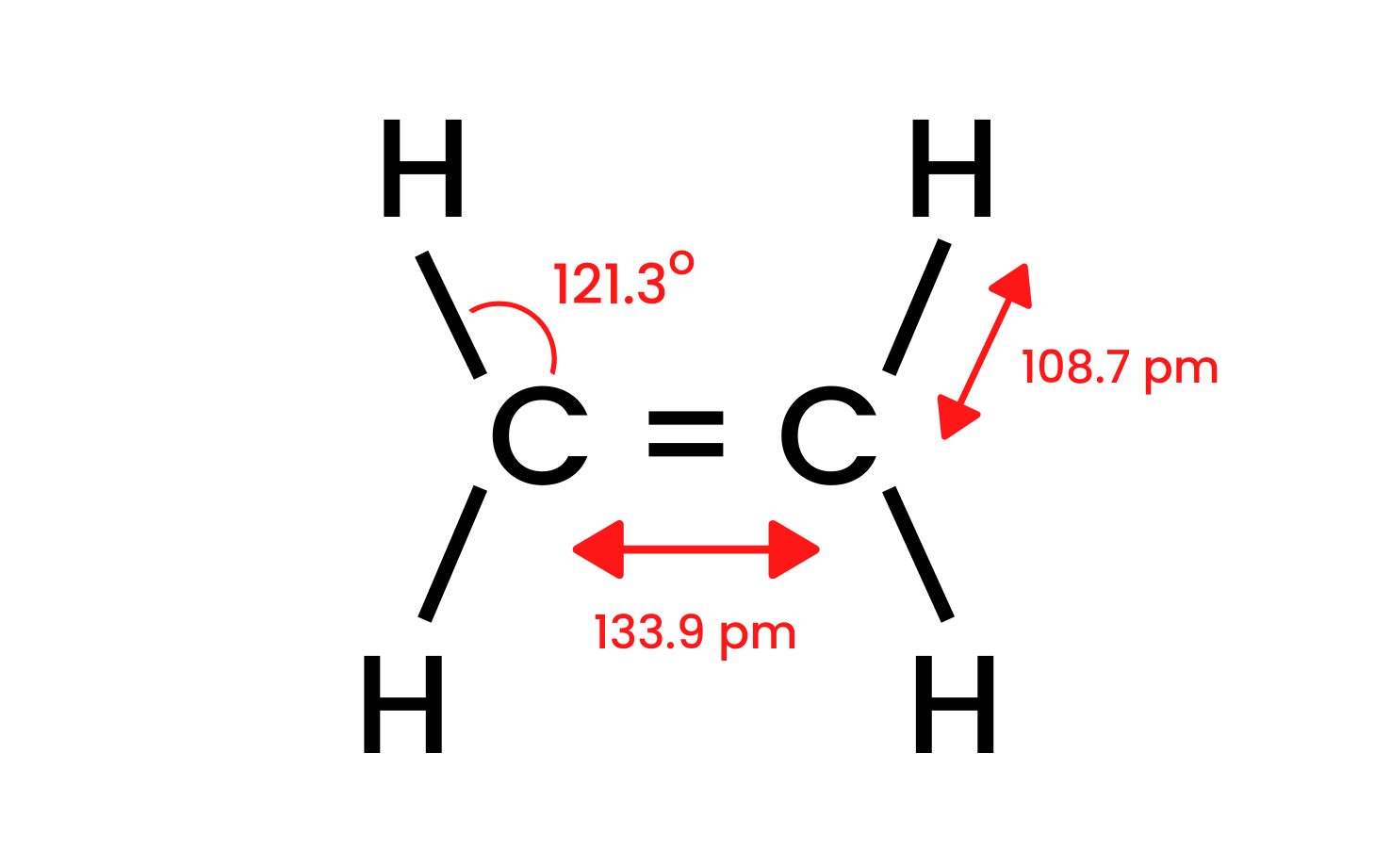
se značí n, vyjadřuje energii elektronu. Nabývá hodnot 1 až 7. Orbitaly, které mají stejné hlavní kvantové číslo, tvoří jednu elektronovou vrstvu. Atomy dosud známých prvků obsazují elektrony 7 elektronových vrstev, které se označují čísly 1 až 7 nebo písmeny K,L,M,N,O,P,Q.Molekula je nejmenší částice látky, která má všechny fyzikální a chemické vlastnosti dané látky. Molekuly se skládají ze dvou nebo více atomů. Atomy tvořící molekulu mohou být stejné (např. molekula kyslíku má dva atomy kyslíku, O2) nebo různé (molekula vody má dva atomy vodíku a jeden atom kyslíku, H2O).
Co je to substituce v chemii : Substituční reakce (latinsky substituere, česky nahradit) je chemická reakce, při které je atom nebo funkční skupina v molekule nahrazen jiným atomem nebo skupinou. Násobnost vazby se při těchto reakcích nemění.